मातीचा पीएच- परिचय
मातीत असलेल्या पाण्यात किती प्रमाणात अन्नद्रव्ये विरघळतील याचे परिमाण म्हणजे पीएच. मातीतल्या पाण्यात किती प्रमाणात हायड्रोजन आयन्स आहेत हे पीएच आपल्याला दाखवतो. मातीचा पीएच हा स्थायी टिकणारा गुणधर्म नाही. मुळांच्या श्वासोश्वास, पिकाच्या व्दारा उचलली जाणारी खते, आपण देत असलेले पाणी, पिकाची वाढीची अवस्था यांच्या मुळे अनेकदा पीएच हा कमी होत असतो.
Video lesson
No video for this lesson.
मातीचा पीएच- परिचय
पीएच म्हणजे काय?मातीचा pH म्हणजे तिचा सामू, म्हणजेच माती आम्लीय आहे की तटस्थ की क्षारीय, हे सांगणारे मापन.
हे मापन ईलेक्ट्रिकल pH मीटर किंवा pH पेपर वापरून केले जाते. pH तपासताना मातीच्या द्रावणाचा pH घेतला जातो.
pH स्केल ० ते १४ अशी असते:
-
७ = तटस्थ (Neutral)
-
७ पेक्षा कमी = आम्लीय (Acidic)
-
७ पेक्षा जास्त = विम्ल/क्षारीय (Alkaline)
pH हा मातीतील हायड्रोजन आयन (H⁺) च्या प्रमाणाचा निगेटिव्ह लॉग आहे. मातीतील हायड्रोजन आयन्स चे प्रमाण हे अतिशय अल्प असल्याने निगेटिव्ह लॉग काढला जातो. यामुळे pH चे मूल्य साधे मापन नसून लघुगणकीय स्वरूपाचे (log scale) आहे.
pH 8 असलेली माती ही pH 7 पेक्षा 10 पट अधिक विम्ल (अल्कली) असते.
म्हणजे pH मध्ये 1 unit वाढ = 10 पट बदल.
आपण अनेकदा pH ला “क्षारता” म्हणून संबोधतो, पण हे पूर्णपणे शास्त्रीयदृष्ट्या बरोबर नाही.
-
pH फक्त हायड्रोजन आयन्सचे प्रमाण दाखवतो.
-
जमीनीत कोणते क्षार, कोणती रासायनिक संयुगे, किती प्रमाणात आहेत—हे pH सांगत नाही.
-
क्षारतेसाठी EC (ईलेक्ट्रिकल कंडक्टिविटी), CEC (कॅटायन एक्सचेंज कॅपेसिटि) आणि Base Saturation पाहणे आवश्यक असते.
म्हणूनच:
pH = H⁺ आयनांचे मापन
क्षारता = जमिनीत असलेल्या विविध क्षारांचे एकूण प्रमाण
ही दोन्ही गोष्टी वेगळ्या आहेत.
४. pH समजल्याने काय फायदा?pH आणि क्षारता यातील फरक समजल्यानंतर:
-
आपण pH बद्दल अनाठायी चिंता करत नाही
-
जमिन सुधारण्यासाठी योग्य उपाय योजना करता येतात
-
खते कमी वापरून जास्त उत्पादन मिळवता येते
-
पोषक घटकांच्या उपलब्धतेचा स्वच्छ अंदाज येतो
खाली दिलेले घटक pH वर मूलभूत परिणाम करतात आणि हे घटक सहज बदलता येत नाहीत.
(A) मातीचा प्रकार (Soil Type)| प्रकार | क्ले | pH |
|---|---|---|
| अँल्युव्हियल | 30–40% | 6.0–8.0 |
| काळी माती | 30–69% | 7.5–8.5 |
| लाल माती | 14–53% | ७ पेक्षा कमी |
स्पष्टीकरण:
जमिनीचा पोत (Texture), म्हणजे क्ले-स्लिट-सॅण्ड यांचे प्रमाण, परिसराचे तापमान, पाऊसमान, मूळ खडक, यावर नैसर्गिक pH ठरलेला असतो.
(B) पाऊस (Rainfall)ज्या भागात पाऊस जास्त, तिथे pH कमी होण्याची प्रवृत्ती:
-
पावसामुळे कॅल्शियम आणि मॅग्नेशियम सारखे base cations काहीप्रमाणात वाहून जातात
-
जमिनीत H⁺ आणि Al³⁺ वाढून pH कमी होतो
-
पावसाचे पाणी स्वतःच थोडे आम्लीय असते (pH 5.7)
Chemical Explanation:
CO₂ + H₂O → H₂CO₃ → H⁺ + HCO₃⁻
हा H⁺ मातीतील Ca²⁺ ला ढकलून बाहेर काढतो, आणि Ca²⁺ HCO₃⁻ सोबत मिळून Ca(HCO₃)₂ बनवतो, जो पावसाबरोबर जमिनीखाली वाहून जातो.
परिणाम → pH कमी.
-
कमी सेंद्रिय पदार्थ असलेल्या जमिनीत pH मध्ये बदल सहज होतो.
-
जास्त सेंद्रिय पदार्थ असलेल्या जमिनीत pH बदल रोखला जातो (buffering).
-
सेंद्रिय पदार्थ वाढविल्यास acidity/alkalinity चा ताण कमी होतो.
काही खते pH कमी करतात (acidifying), काही वाढवतात (alkalizing).
(A) pH कमी करणारी खते (Acid-forming fertilizers)| खत | N% | pH वर परिणाम |
|---|---|---|
| अमोनियम नायट्रेट | 33% | आम्ल |
| अमोनियम सल्फेट | 20–21% | अत्यंत आम्ल |
| युरिया | 46% | आम्ल |
| डि ए पी | 18% | मध्यम आम्ल |
साधे स्पष्टीकरण:
अमोनियम (NH₄⁺) चे नायट्रेटमध्ये (NO₃⁻) रूपांतर होताना H⁺ तयार होतो → pH कमी होतो.
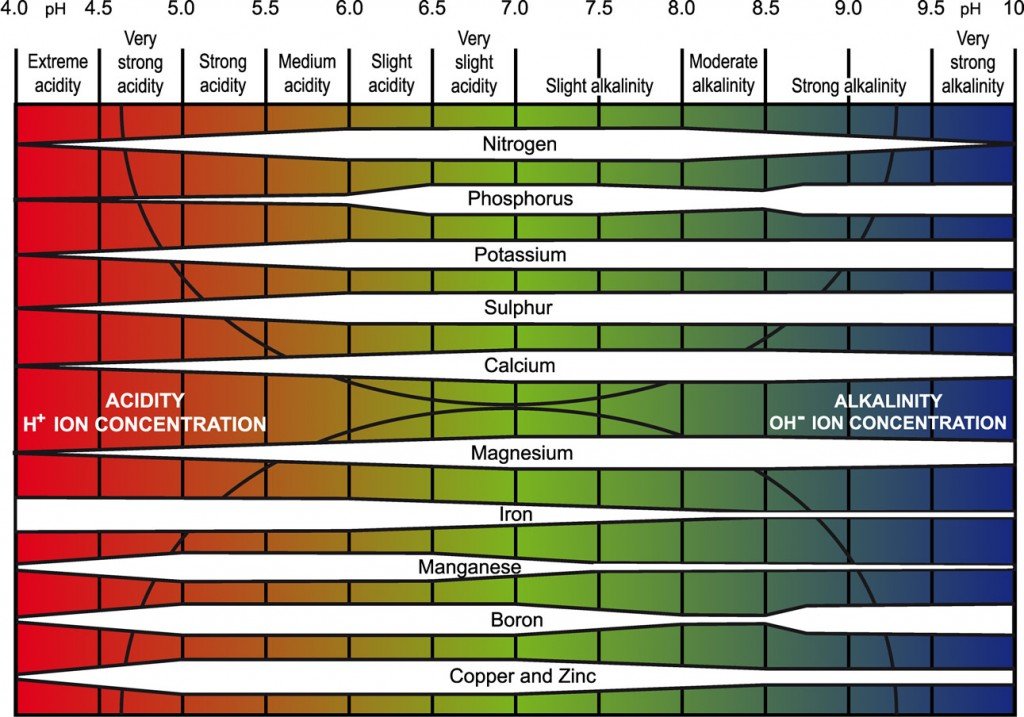
७. pH आणि पोषकद्रव्यांची उपलब्धताpH हा पिकांना उपलब्ध होणाऱ्या पोषकद्रव्यांचा “दरवाजा उघडा/बंद” करणारा घटक आहे. पीएच हा अन्नद्रव्ये किती प्रमाणात विरघळतात हे ठरवणारा घटक म्हणजे पीएच असतो. जसा जसा पीएच कमी होत जातो तसा मातीची ईसी वाढत जातो. आपण ईसी या भागात याबाबत सविस्तर माहीती घेणार आहोत. खालिल माहीतीचा सविस्तर अभ्यास केला तर लक्षात येईल की, मातीचा पीएच कमी करणे हे काहीही गरजेचे नाही. आपण मातीचा, पाण्याचा पीएच कमी करण्यासाठी जो प्रयत्न करतो त्यातुन एक नविन समस्या निर्माण होते की, पिक ताणाखाली जाते. जेव्हा आपल्याला पीएच किती कमी करायचा आणि केव्हा करायचा हे पुर्णपणे कळलेले असते, तेव्हाच मातीचा पीएच कमी करणारी क्रिया करणे योग्य ठरते, अन्यथा ती एक दुधारी तलवार म्हणुन सिध्द होते.
नायट्रोजन (N)
-
pH 5.5–8.5 मध्ये उपलब्ध.
-
या पलिकडे कमी.
फॉस्फोरस (P)
-
सर्वोत्तम 6.0–7.5
-
pH 8.5 नंतरही थोडा उपलब्ध
-
अत्यंत उच्च pH (9.5–10) पर्यंतही काही प्रमाणात उपलब्ध
पोटॅश (K)
-
pH 7.5 नंतर उपलब्धता कमी → 8.5 पलीकडे पुन्हा वाढते
-
pH 10 पर्यंत ठीकठाक उपलब्ध
सल्फर (S) व मॉलिब्डेनम (Mo)
-
6.5 ते 10 पर्यंत उपलब्ध
कॅल्शियम (Ca), मॅग्नेशियम (Mg)
-
pH 6–9 = स्थिर उपलब्धता
-
pH 9 नंतर कमी
बोरॉन (B)
-
5–7.5 = सर्वोत्तम
-
7.5 नंतर जवळपास शून्य
-
काही परिस्थितीत 8.5 नंतर थोडा वाढ
फेरस (Fe)
-
4.5–6.5 = जास्त
-
pH वाढला की उपलब्धता अचानक कमी
कॉपर व झिंक (Cu/Zn)
-
5–8 = उपलब्ध
-
pH वाढल्यावर कमी
Supporting files
No files available for this lesson.